| 此条目需要补充更多来源。 (2016年10月1日) |
氩(拼音:yà,注音:丨ㄚˋ,粤拼:aa3; 英语:Argon),是一种化学元素,其化学符号为Ar,原子序数为18,原子量为39.948 u,位在周期表的第18族,是一种稀有气体[2]。氩占大气体积的0.934%(9340 ppmv),是地球大气层第三多的气体,是水蒸气的两倍以上(平均4000 ppmv左右,但变化很大)、二氧化碳(400 ppmv)的23倍之多、氖(18 ppmv)的500倍以上。氩是地壳含量中最丰富的惰性元素,在地壳中占了0.00015%。[3]
氩(来自希腊语ἀργόν,带有懒惰或无效的意思),命名是参考它的化学活性。这个第一个被发现的稀有气体的化学性质令命名者印象深刻。[4][5]1785年,亨利·卡文迪什怀疑稀有气体是组成大气的一部分气体。1894年,在伦敦大学学院, 约翰·斯特拉特,第三代瑞利男爵和威廉·拉姆齐透过移除了氧气、二氧化碳、水以及氮的干净空气样本,使氩第一次从空气里被隔绝出来。[6][7][8] 他们已经确认从化学化合物生成的氮比大气中的氮还要轻0.5%,差异细微,但已足够重要吸引他们的注意力好几个月。他们做出了结论:空气中还有另一种气体与氮气混和在一起。[9]氩气在1882也被H. F. Newall和沃尔特·诺尔·赫特利的研究偶然发现。他们发现新的发射光谱,并没有符合在当时已经知道的元素。 直到1957年,氩的化学符号一直是"A",之后被改为"Ar"到现在。[10]
氩,是一种稀有气体。无论是气态还是液态,都是无色、无味而且无毒。它在水中的溶解度比氮多出了2.5倍。虽然氩在一般的情况下都很稳定,不会与其它化合物或元素化合,但是科学家还是有办法在极端的条件下形成一些氩化合物,像是2000年8月由芬兰化学家马库·拉萨能(Markku Räsänen)领导的小组发现的氟氩化氢()。这个氟、氢和氩的化合物在−265°C才能保持稳定。[11]此外,氩还可以作为客体分子,与水形成包合物。[12]除了以上基态的物质外,目前已经发现含氩的离子和激发态配合物(像ArH+和ArF),而根据理论计算显示氩应该可以形成在室温下稳定的化合物,虽然目前还没有发现它们存在的线索。[13]
氩在地球大气中的含量以体积计算为0.934%,而以质量计算为1.29%,在地壳中,由于氩在自然情况下不与其他化合物反应,而无法形成固态物质,但可以被“困在”放射性岩石中。鉴于空气中的氩更易得,工业用的氩大多就直接从空气中提取。主要是用分馏法提取,而像是氮、氧、氖、氪、氙等气体也都是这样从空气中提取的。 [18] 而在火星的大气中,氩-40以体积计算的话占有1.6%,而氩-36的浓度为5ppm;另外1973年水手号计划的太空探测器飞过水星时,发现它稀薄的大气中占有70%氩气,科学家相信这些氩气是从水星岩石本身的放射性同位素衰变而成的。卡西尼-惠更斯号在土星最大的卫星,也就是泰坦上,也发现少量的氩。[19]
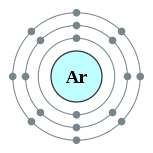
由于氩气拥有的八个价电子,占满了其原子轨道的最外层,因此不容易与其他的原子结合,化学性质非常不活泼。在1962年以前,一般认为氩和其他的稀有气体是完全无法与其他物质产生化学反应,但不久之后比氩重的氙和氪的化合物就陆续被合成,因此也激励了科学家发现新的稀有气体化合物。1982年在星际空间探测到氩氢离子,是氩的一种多原子离子。[21]在2000年8月,第一个氩的化合物在芬兰的赫尔辛基大学由马库·拉萨能领导的小组首先被制备出来,他们利用紫外线照射含有微量氟化氢的氩气冰块,形成了氟氩化氢,分子式为HArF,这种化合物可以在40K(−233℃)的低温下保持稳定。[22]另外在2003年发现了一种新氩化合物存在的踪迹,二氟化氩(ArF2)[来源请求],但目前还没有任何可靠的证据可以证实。
工业上
目前在工业上得到氩的方法就是把空气蒸馏。用冷凝器可以先把沸点90.2K的氧液化,移除液氧之后继续冷却就可以液化沸点为87.3K的氩气,最后留下沸点77.35K的氮气。目前以这种方法制造的氩气在全世界高达七十万吨/年。[23]
其他方法

因为氩气具有惰性、低传热率等性质,因此它被广泛地运用在许多方面。[24]
氩气最主要的用处就是它的惰性,可以保护一些容易与周遭物质发生反应的东西。[24]虽然其他的稀有气体也有这些特性,但是氩气在空气中的含量最多,也是最容易取得,因此相对就比较便宜,具有经济效益。另外氩气便宜的原因还有它是制造液氧和液氮的副产品,而由于它们两个都是工业上重要的原料,生产很多,所以每年都有很多的液氩副产品。[来源请求]
以氩惰性的用途主要有:
- 电灯泡里的填充气体,由于氩气不会与灯芯产生化学反应,而又能保持气压减缓钨丝升华,可延长灯丝使用寿命。
- 氩可当作焊接时所用的保护气体,其中包括MIG焊接、GTA焊接与GMA焊接等,在这时氩通常会和二氧化碳混合在一起使用。[25]
- 可用于灭火,用氩气灭火的好处是几乎不会破坏任何火场的物品,通常使在火场有特殊仪器时才使用。
- 是用于感应耦合等离子体的气体之一。[26]
- 用于保护加工中的钛和其他容易发生反应的金属:例如铷 和铯 。
- 保护成长中的硅晶体和锗晶体,这晶体主要用于半导体学。
- 在博物馆里,会在一些重要文物的玻璃专柜里填充氩气,避免氧化。[27]
- 在啤酒罐中的填充物,虽然也可以用氮气代替。
- 在酿酒的过程中,啤酒桶里的填充物,它可以把氧气置换,以避免啤酒桶里的原料被氧化成乙酸。
- 在药学里,氩可以用于保护一些静脉内的治疗的药物,举个例子,像是对乙酰氨基酚。一样的,这也是防止药物受到氧气的破坏。
- 用于冷却AIM-9响尾蛇导弹的追踪器,氩当时都是以高压储存,然后当释放气体后就可以带走一些热量。[28]
- 为石墨电熔炉中的保护气体,以免它被氧化。
- 广告用的霓虹灯里,有时也会加入氩气,加了氩气的霓虹灯管,白天看起来是无色透明的,一旦通电后,氩气受到电的刺激,会放出青色的光芒。
- 氩气的低传热率也是它的特性之一,像它可以作为隔热窗户中两层玻璃之间的填充物。[29]
- 因为氩的低传热率和惰性,氩气在水肺潜水可以用来作为膨胀潜水衣的气体。氩气还可以在水肺中代替氮气(吸收纯氧对身体不好,因此水肺中要添加其他气体),因为氮气在高压下会溶进血液里而造成氮麻醉,氩气则可以减轻这种症状(虽然一般来说,稀有气体也会造成这种症状)。[30]
- 元素氩在洛斯阿拉莫斯国家实验室的介绍(英文)
- EnvironmentalChemistry.com —— 氩(英文)
- 元素氩在The Periodic Table of Videos(诺丁汉大学)的介绍(英文)
- 元素氩在Peter van der Krogt elements site的介绍(英文)
- WebElements.com – 氩(英文)
- (英文) Emsley, J., Nature’s Building Blocks; Oxford University Press: Oxford, NY, 2001; pp. 35–39.
- (英文) Brown, T. L.; Bursten, B. E.; LeMay, H. E., In Chemistry: The Central Science, 10th ed.; Challice, J.; Draper, P.; Folchetti, N. et al.; Eds.; Pearson Education, Inc.: Upper Saddle River, NJ, 2006; pp. 276 and 289.
- (英文) Triple point temperature: 83.8058 K - Preston-Thomas, H. The International Temperature Scale of 1990 (ITS-90). Metrologia. 1990, 27: 3–10 [2008-05-05]. (原始内容存档于2011-04-20).
- (英文) Triple point pressure: 69 kPa - Section 4, Properties of the Elements and Inorganic Compounds; Melting, boiling, triple, and critical temperatures of the elements. CRC Handbook of Chemistry and Physics 85th edition. Boca Raton, Florida: CRC Press. 2005.
- ^ Magnetic susceptibility of the elements and inorganic compounds 互联网档案馆的存档,存档日期2012-01-12., in Handbook of Chemistry and Physics 81st edition, CRC press. ,archive-web,archive-is
- ^ In older versions of the periodic table, the noble gases were identified as Group VIIIA or as Group 0. See Group (periodic table).
- ^ 存档副本. [2020-02-04]. (原始内容存档于2020-02-03).
- ^ Hiebert, E. N. In Noble-Gas Compounds. Hyman, H. H. (编). Historical Remarks on the Discovery of Argon: The First Noble Gas. University of Chicago Press. 1963: 3–20.
- ^ Travers, M. W. The Discovery of the Rare Gases. Edward Arnold & Co. 1928: 1–7.
- ^
Lord Rayleigh; Ramsay, William. Argon, a New Constituent of the Atmosphere. Proceedings of the Royal Society. 1894–1895, 57 (1): 265–287. JSTOR 115394. doi:10.1098/rspl.1894.0149
 .
.
- ^
Lord Rayleigh; Ramsay, William. VI. Argon: A New Constituent of the Atmosphere. Philosophical Transactions of the Royal Society A. 1895, 186: 187–241. Bibcode:1895RSPTA.186..187R. JSTOR 90645. doi:10.1098/rsta.1895.0006
 .
.
- ^ Ramsay, W. Nobel Lecture. The Nobel Foundation. 1904 [2008-05-02]. (原始内容存档于2017-11-17).
- ^ About Argon, the Inert; The New Element Supposedly Found in the Atmosphere. The New York Times. 3 March 1895 [1 February 2009]. (原始内容存档于2016-03-04).
- ^ Holden, N. E. History of the Origin of the Chemical Elements and Their Discoverers. National Nuclear Data Center. 12 March 2004 [2008-05-02]. (原始内容存档于2011-07-21).
- ^ Khriachtchev, Leonid; Mika Pettersson, Nino Runeberg, Jan Lundell & Markku Räsänen. A stable argon compound. Nature. 2000-08-24, 406: 874–876 [2008-05-01]. doi:10.1038/35022551. (原始内容存档于2016-04-13).
- ^ Belosludov, V. R.; O. S. Subbotin, D. S. Krupskii, O. V. Prokuda, and Y. Kawazoe. Microscopic model of clathrate compounds (PDF). Institute of Physics (has blown up once in a while) Publishing: 1. 2006 [2007-03-08] (英语). [永久失效链接]
- ^ Cohen, A.; Lundell, J.; Gerber, R. B. First compounds with argon–carbon and argon–silicon chemical bonds. Journal of Chemical Physics. 2003, 119 (13): 6415. Bibcode:2003JChPh.119.6415C. doi:10.1063/1.1613631.
- ^ "Periodic Table of the Elements: Argon Archived 2011-08-22 at WebCite. ,archive-web,archive-is" Lenntech (页面存档备份,存于互联网档案馆). 2008. Retrieved on September 3, 2007.
- ^ Lord Rayleigh;William Ramsay . Argon, a New Constituent of the Atmosphere.. Proceedings of the Royal Society of London. 1894–1895, 57 (1): 265–287.
- ^ William Ramsay. Nobel Lecture in Chemistry, 1904. [2008-05-02]. (原始内容存档于2017-11-17).
- ^ Holden, Norman E. History of the Origin of the Chemical Elements and Their Discoverers. National Nuclear Data Center (NNDC). 12. (原始内容存档于2011-07-21) (英语). 已忽略未知参数
|month=(建议使用|date=) (帮助); - ^ Argon, Ar. [2007-03-08]. (原始内容存档于2008-10-07).
- ^ Seeing, touching and smelling the extraordinarily Earth-like world of Titan. European Space Agency. 21. (原始内容存档于2008-05-13) (英语). 已忽略未知参数
|month=(建议使用|date=) (帮助); - ^ 20.0 20.1 40Ar/39Ar dating and errors. [2007-03-07]. (原始内容存档于2007-10-14).
- ^ Brault, James W; Davis, Sumner P. Fundamental Vibration-Rotation Bands and Molecular Constants for the ArH+ Ground State (1Σ+ ). Physica Scripta. 1 February 1982, 25 (2): 268–271. Bibcode:1982PhyS...25..268B. doi:10.1088/0031-8949/25/2/004.
- ^ Bartlett, Neil. The Noble Gases. Chemical & Engineering News. (原始内容存档于2018-04-29) (英语).
- ^ 氩的介绍
- ^ 24.0 24.1 存档副本. [2020-06-30]. (原始内容存档于2020-06-30).
- ^ Weman, p 53
- ^ 感應耦合電漿離子質譜儀技術及其在材料分析的運用 (PDF). 李珠. [2008-05-03]. (原始内容 (PDF)存档于2019-09-03).
- ^ USA National Archives description of how the Declaration of Independence is stored and displayed (页面存档备份,存于互联网档案馆). More detail can be found in this more technical explanation 互联网档案馆的存档,存档日期2008-01-02., especially Page 4 (页面存档备份,存于互联网档案馆), which talks about the argon keeping the oxygen out.
- ^ Description of Aim-9 Operation 互联网档案馆的存档,存档日期2008-12-22. ,archive-web,archive-is
- ^ Energy-Efficient Windows. Bc Hydro. [2007-03-08]. (原始内容存档于2007-02-02).,archive-web,archive-is
- ^ "氮麻醉"。 大英百科全书。 2008年。 大英线上繁体中文版。2008年5月4日 <[1][永久失效链接],archive-web,archive-is>.
- ^ Fujimoto, James; Rox Anderson, R. Tissue Optics, Laser-Tissue Interaction, and Tissue Engineering (PDF). Biomedical Optics: 77–88. 2006 [2007-03-08]. (原始内容 (PDF)存档于2006-03-14) (英语). ,archive-web,archive-is
- ^ 鉀-氬年代測定法. 中国大百科智慧藏. [2008-05-05]. (原始内容存档于2008-10-24).,archive-web,archive-is
- ^ Middaugh, John; Bledsoe, Gary. "Welder's Helper Asphyxiated in Argon-Inerted Pipe (FACE AK-94-012) 互联网档案馆的存档,存档日期2008-04-17.,archive-web,archive-is." State of Alaska Department of Public Health (页面存档备份,存于互联网档案馆). June 23, 1994. Retrieved on September 3, 2007.
- 元素氩在洛斯阿拉莫斯国家实验室的介绍(英文)
- EnvironmentalChemistry.com —— 氩(英文)
- 元素氩在The Periodic Table of Videos(诺丁汉大学)的介绍(英文)
- 元素氩在Peter van der Krogt elements site的介绍(英文)
- WebElements.com – 氩(英文)


 )。这个
)。这个 (在1957年以前,它的符号为
(在1957年以前,它的符号为 )。
)。 )天然含量99.6%、 氩-36(
)天然含量99.6%、 氩-36( )天然含量0.34%和氩-38(
)天然含量0.34%和氩-38( )天然含量0.06%。一般来说稳定的氩-40是由
)天然含量0.06%。一般来说稳定的氩-40是由 )经由
)经由 )。这个特性可以被用来测定
)。这个特性可以被用来测定 )可经由
)可经由 )的
)的 )
)
