钡(拼音:bèi,注音:ㄅㄟˋ,粤拼:bui3;英语:Barium;源于希腊语:βαρύς,转写为barys,直译为重的;),是一种化学元素,其化学符号为Ba,原子序数为56,原子量为137.327 u。钡是元素周期表中2A族的第五个元素,是一种柔软的有银白色金属光泽的碱土金属。由于它的化学性质十分活泼,从来没有在自然界中发现钡单质。
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 外观 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
银白色金属 钡金属 钡的原子光谱 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 概况 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 名称·符号·序数 | 钡(Barium)·Ba·56 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 元素类别 | 碱土金属 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 族·周期·区 | 2 ·6·s | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 标准原子质量 | 137.327 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 电子排布 | [氙] 6s2 2,8,18,18,8,2  | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 历史 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 发现 | 卡尔·威廉·舍勒(1772年) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 分离 | 汉弗里·戴维(1808年) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 物理性质 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 物态 | 固态 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 | (接近室温) 3.51 g·cm−3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 熔点时液体密度 | 3.338 g·cm−3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 熔点 | 1000 K,727 °C,1341 °F | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 沸点 | 2170 K,1897 °C,3447 °F | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 熔化热 | 7.12 kJ·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 汽化热 | 140.3 kJ·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 比热容 | 28.07 J·mol−1·K−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
蒸气压
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子性质 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 氧化态 | +2 (强碱性) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 电负性 | 0.89(鲍林标度) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 电离能 | 第一:502.9 kJ·mol−1 第二:965.2 kJ·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子半径 | 222 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 共价半径 | 215±11 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 范德华半径 | 268 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 杂项 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 晶体结构 | 体心立方 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 磁序 | 顺磁性 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 电阻率 | (20 °C)332 n Ω·m | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 热导率 | 18.4 W·m−1·K−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 膨胀系数 | (25 °C)20.6 µm·m−1·K−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 杨氏模量 | 13 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 剪切模量 | 4.9 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 莫氏硬度 | 1.25 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS号 | 7440-39-3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 最稳定同位素 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
主条目:钡的同位素
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
钡在自然界中最常见的矿物是重晶石(硫酸钡,BaSO4)和毒重石(碳酸钡,BaCO3),二者皆不容于水。它在1774年被确认为一个新元素,但直到1808年电解法发明不久后才被归纳为金属元素。
钡在工业上只有少量应用。过去曾用它作为真空管中的吸气剂。它是YBCO(一种高温超导体)和电瓷的成分之一,也可以被添加进钢中来减少金属构成中碳颗粒的数量。钡的化合物用于制造烟火中的绿色。硫酸钡作为一种不溶的重添加剂被加进钻井液中,而在医学上则作为一种X光造影剂。可溶性钡盐因为会电离出钡离子所以有毒,因此也被用做老鼠药。

物理性质
钡是一种软的银白色金属,在极纯时稍带有金色。[1]:2 钡金属的银白色会因在空气中氧化而快速消失,产生一层暗灰色的氧化层。钡有中等的单位重和良好的导电性。极纯的钡非常难以制备,所以钡的很多特性还未能准确的测量。[1]:2
在室温与常压下,钡呈立方晶系,钡原子间的距离为503皮米,并在每秒1.8×10-5 °C的加热速度下膨胀。[1]:2 它是一种非常软的金属,其摩氏硬度为1.25。[1]:2 它的熔点为1,000 K(730 °C)[2]:4–43,介于锶的1,050 K(780 °C)[2]:4–86与镭的973 K(700 °C)[2]:4–78之间。但是它的沸点2,170 K(1,900 °C)超过了锶的熔点1,655 K(1,382 °C)[2]:4–86。 它的密度(3.62 g·cm−3)[2]:4–43仍然在锶的(2.36 g·cm−3)[2]:4–86和镭的(~5 g·cm−3)之间。[2]:4–78
化学性质
钡的化学性质与镁、钙和锶相似。在大多数情况下,钡的氧化态为+2。由于钡单质可与氧族元素发生反应放出大量热量,为了防止与空气中的氧气发生反应,钡单质一般储存于油或惰性气体中。[1]:2钡单质在加热时亦可与其它非金属单质发生放热反应。[1]:2-3
钡也可以与水或醇发生反应放出氢气:
钡可以与氨发生反应形成配合物,如Ba(NH3)6。[1]:3
钡易与酸发生反应生成盐。然而钡遇硫酸时会反应生成不溶于水的硫酸钡,从而使反应停止。[3]
钡可以与铝、锌、铅、锡等金属形成金属互化物及合金。[4]
化合物
钡离子没有特别的颜色,因此钡盐通常显白色,其溶液为无色。[5]钡盐的密度通常比同类的钙盐和锶盐更大,参见下表。(表中锌盐供对比参考)
| O2− | S2− | F− | Cl− | SO2−4 | CO2−3 | O2−2 | H− | |
|---|---|---|---|---|---|---|---|---|
| Ca2+ [2]:4–48–50 | 3.34 | 2.59 | 3.18 | 2.15 | 2.96 | 2.83 | 2.9 | 1.7 |
| Sr2+ [2]:4–86–88 | 5.1 | 3.7 | 4.24 | 3.05 | 3.96 | 3.5 | 4.78 | 3.26 |
| Ba2+ [2]:4–43–45 | 5.72 | 4.3 | 4.89 | 3.89 | 4.49 | 4.29 | 4.96 | 4.16 |
| Zn2+ [2]:4–95–96 | 5.6 | 4.09 | 4.95 | 2.09 | 3.54 | 4.4 | 1.57 | — |
炼金术士最早通过加热碳酸钡得到氢氧化钡。与氢氧化钙不同,氢氧化钡溶液不易吸收二氧化碳,因此常用于校准pH检测设备。
同位素
钡有40种已知的同位素,质量数介于114和153之间,其中有6种是稳定的(钡-132、134至138),其他都具有放射性。
在地壳中可以找到7种钡的同位素,分别是稳定的钡-132、134至138和具微弱放射性的钡-130。[6]其同位素质量越小,丰度越低。在所有稳定同位素中,丰度最高的是钡-138,占自然界中钡的71.7%。[6]钡-130会发生双正β衰变缓慢衰变成氙-130 ,半衰期长达(0.5–2.7)×1021年(约为宇宙年龄的1011倍),其丰度约占天然钡的0.1%。[6]理论上,钡-132亦可借由双β衰变转变成氙-132,但尚未观测到其发生。[7]这两种同位素的放射性都微乎其微,不会对生命构成任何威胁。
最稳定的人造放射性同位素是钡-133,半衰期约为10.51年。其他人造同位素中有五种的半衰期超过一天。[7]钡有10个亚稳态同核异构体,其中以钡-133m1最为稳定,半衰期约39小时。[7]

中世纪初,炼金术士即对一些钡矿石有所了解。在意大利博洛尼亚发现的一些被称为“博洛尼亚石”的平滑卵石状重晶石块曾得到炼金术士的注意,因为这些矿石在受到光照后会发光数年。1602年,卡西奥劳罗(V. Casciorolus)描述了这种用有机物加热重晶石发出磷光的性质。[1]:5
1774年,卡尔·威廉·舍勒发现重晶石中含有一种未发现的新元素,但无法分离提纯这种元素,只能得到它的氧化物,即氧化钡。两年后,约翰·戈特利布·甘恩也在相同的研究中得到了氧化钡。氧化钡最早被Guyton de Morveau称作“barote”,后来被拉瓦锡改作“baryta”。同在18世纪,英国矿物学家威廉·威灵宁在坎伯兰的铅矿中注意到一种沉重的矿物,现在称为毒重石,其主要成分为碳酸钡。1808年,汉弗里·戴维首次通过电解熔融的钡盐分离钡单质。[8]戴维通过与钙类似的命名方法,用重晶石(baryta)的名称加上表示元素的后缀-ium来命名钡(barium)。[9]罗伯特·本生与奥古斯都·马修森通过电解氯化钡和氯化铵的熔融混合物来获得纯钡。[10][11]
在20世纪初的液化空气电解分馏技术出现之前,从1880年代开始,纯氧一般通过过氧化钡的分解来生产。此方法的原理是,将氧化钡在空气中加热到500-600 °C(932-1,112 °F)生成过氧化钡,然后将过氧化钡加热到700 °C(1,292 °F)以上分解释放氧气:[12][13]
从1908年开始,硫酸钡被用作X光检测消化系统时使用的造影剂。[14]
钡在地壳中的含量为0.0425%,海水中为13μg/ L。钡的生产主要依靠世界各地的硫酸钡矿物重晶石。钡也可以通过碳酸钡矿物毒重石来生产,此类矿物主要储藏于英国、罗马尼亚和前苏联。[1]:5

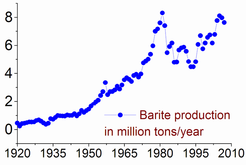
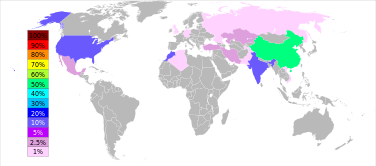
重晶石的估计储量在0.7至20亿吨之间。重晶石的年产量最大为1981年的830万吨。自1990年代下半叶开始,重晶石生产从1996年的560万吨增加到2005年的7.6%,在2011年达到7.8%。中国占重晶石产量的50%以上,其次是印度(2011年为14%)、摩洛哥(8.3%)、美国(8.2%)、土耳其(2.5%)、伊朗和哈萨克斯坦(各占2.6%)。[15]
开采出的矿石需要经过洗涤、粉碎、分类,并与石英分离。如果石英渗入矿石过深,或者矿石中铁、锌、铅含量过高,则须使用泡沫浮选法处理。最终得到的产物是质量分数98%的重晶石,纯度不低于95%,且铁和二氧化硅含量极少。[1]:7随后使用碳还原硫酸钡:
生成了水溶性的硫化钡之后,便可以作为其它产品的原料:与氧反应得到硫酸钡,与硝酸生成硝酸钡,与二氧化碳生成碳酸钡等。硝酸钡加热分解可以产生钡的氧化物。金属钡可以用氧化钡在1,100 °C(2,010 °F)下与铝反应得到。其中首先生成金属互化物BaAl4:
BaAl4是与氧化钡反应生成金属的中间产物。注意并非全部钡元素都被还原。
剩余的氧化钡与生成的氧化铝反应:
总反应为:[1]:3
钡蒸气在氩气气氛中冷凝并装入模具中。这种方法在商业上用于生产超纯钡。通常市面上出售的钡纯度约99%,主要杂质为锶和钙(含量达到0.8%和0.25%),而其他杂质成分小于0.1%。
硫酸钡与硅在1,200 °C(2,190 °F)下亦可发生类似的反应得到钡和偏硅酸钡。但工业上一般不会使用电解法,因为钡易溶于熔融的卤化物,并且产物纯度较低。[1]:3
宝石
蓝锥矿为钡矿物,是一种非常罕见的蓝色荧光宝石,被其发现地加利福尼亚州定为州石。
金属单质及其合金
钡单质或钡铝合金可用于吸收真空管(如电视显像管)中的多余气体。钡因其氧气,氮气,二氧化碳和水的蒸气压和反应度较低而适用于此目的。它甚至可以通过溶解于在晶格中来部分去除惰性气体。随着液晶显示器和等离子显示器的日益普及,这种应用现在已较少见。[1]:4
钡单质的其他用途较少见。其中包括:[1]:4
- 添加于硅铝合金中以优化其结构;
- 用作轴承合金;
- 添加到铅锡焊料合金中增加抗蠕变性;
- 添加于用于火花塞的镍合金;
- 添加到钢和铸铁中作为孕育剂;
- 与钙、锰、硅和铝组成合金,用作高级钢脱氧剂。
硫酸钡和重晶石
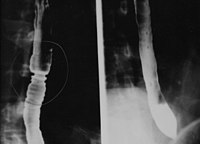
在石油工业中,硫酸钡有十分重要的用途,常用于石油和天然气井中的钻井液。[2]:4-5其沉淀(称为“blanc fixe”,源于法语“永久的白色”)可用于油漆、墨水、塑料或橡胶中,或作为纸张涂料。也可用于纳米颗粒中以改善某些聚合物(如环氧树脂)的物理性质。[1]:9
硫酸钡的毒性较低而密度较大,约为4.5 g/cm3,因此对X光不透明。因此,硫酸钡被用作消化道X光成像中的放射性造影剂(称作“钡餐”)。[2]:4-5立德粉,也称作锌钡白,是一种含有硫酸钡和硫化锌的具有良好遮盖力的永久性白色色素,即使暴露于硫化物中时也不会变暗。[16]
其它钡化合物

与不溶于水的硫酸钡不同,由于溶液中的钡离子Ba2+具有毒性(例如碳酸钡是一种老鼠药),许多钡化合物的应用受到了一定限制。
- 荧光灯电极上的氧化钡涂层有利于电子的释放。
- 由于原子密度较大,碳酸钡提高了玻璃的折射率和光泽[2]:4–5,并可减少阴极射线管(CRT)电视机的X射线泄漏。[1]:12–13
- 加入硝酸钡可使烟花变为黄色或苹果绿;[17]使用一氯化钡则变为亮绿色。
- 过氧化钡可用于焊接轨道的铝热剂中作为催化剂。它也用于曳光弹中以产生绿色光晕。[18]
- 钛酸钡是一种很有前景的电子陶瓷。[19]
- 氟化钡因其0.15-12微米的宽透明度范围,常用于红外应用中的光学器件。[20]
- 钇钡铜氧(YBCO)是第一个用液氮冷却的高温超导体,因为其转变温度为93 K(−180.2 °C;−292.3 °F),超过了氮的沸点(77 K或−196.2 °C或−321.1 °F)。[21]
- 铁氧体是一种由氧化铁(Fe2O3)和氧化钡(BaO)组成的烧结陶瓷材料,绝缘同时又具有亚铁磁性,可以被暂时或永久性磁化。
由于金属钡的高反应性,其毒理性数据仅适用于其化合物。[22]
水溶性的钡化合物有毒。低剂量下的钡离子可以作为肌肉兴奋剂,而较高剂量下钡离子则会影响神经系统,导致心率不整、发抖、虚弱、焦虑、呼吸困难甚至瘫痪。这种毒性可能来源于钡离子阻断了对神经系统至关重要的钾离子通道。[23]水溶性的钡化合物(钡离子)还可以导致其他器官即眼睛、免疫系统、心脏、呼吸系统和皮肤[22]受到损害,如失明或致敏。[22]
钡元素不会致癌[22],也不会生物累积。 [24][25]含有不溶性钡化合物的吸入粉尘在肺部积聚,会导致称为钡尘肺的良性病症。[26]硫酸钡不溶于水,因此是无毒的,在交通运输中不属于危险品。[1]:9
为避免可能发生剧烈的化学反应,金属钡通常保存于氩气氛中或矿物油下。与空气直接接触可能导致自燃。储存时应避免受潮、摩擦、受热、火花、火焰、冲击、静电以及与氧化剂或酸接触。任何可能与钡直接接触的物体都应该先接地处理。使用金属钡的人员应该穿着预先清洁过的无火花鞋、防火橡胶衣服、橡胶手套、围裙、护目镜和防毒面具。禁止在工作场所吸烟。操作后需要进行彻底清洗。[22]
- 硅酸铜钡:古代中国使用的合成钡铜硅酸盐颜料。
- 张培善石(BaFCl):近年新发现的卤化钡矿物。
- ^ 1.00 1.01 1.02 1.03 1.04 1.05 1.06 1.07 1.08 1.09 1.10 1.11 1.12 1.13 1.14 1.15 1.16 1.17 Kresse, Robert; Baudis, Ulrich; Jäger, Paul; Riechers, H. Hermann; Wagner, Heinz; Winkler, Jocher; Wolf, Hans Uwe. Barium and Barium Compounds. Ullman, Franz (编). Ullmann's Encyclopedia of Industrial Chemistry. Wiley-VCH. 2007. doi:10.1002/14356007.a03_325.pub2.
- ^ 2.00 2.01 2.02 2.03 2.04 2.05 2.06 2.07 2.08 2.09 2.10 2.11 2.12 2.13 Lide, D. R. CRC Handbook of Chemistry and Physics 84th. Boca Raton (FL): CRC Press. 2004. ISBN 978-0-8493-0484-2.
- ^ Müller, Hermann. Sulfuric Acid and Sulfur Trioxide. Ullman, Franz (编). Ullmann's Encyclopedia of Industrial Chemistry. Wiley-VCH. 2007. doi:10.1002/14356007.a03_325.pub2.
- ^ Ferro, Riccardo & Saccone, Adriana. Intermetallic Chemistry. Elsevier. 2008: 355. ISBN 978-0-08-044099-6.
- ^ Slowinski, Emil J.; Masterton, William L. Qualitative analysis and the properties of ions in aqueous solution 2nd. Saunders. 1990: 87. ISBN 978-0-03-031234-2.
- ^ 6.0 6.1 6.2 De Laeter, J. R.; Böhlke, J. K.; De Bièvre, P.; Hidaka, H.; Peiser, H. S.; Rosman, K. J. R.; Taylor, P. D. P. Atomic weights of the elements. Review 2000 (IUPAC Technical Report). Pure and Applied Chemistry. 2003, 75 (6): 683–800. doi:10.1351/pac200375060683.
- ^ 7.0 7.1 7.2 Audi, G.; Kondev, F. G.; Wang, M.; Huang, W. J.; Naimi, S. The NUBASE2016 evaluation of nuclear properties (PDF). Chinese Physics C. 2017, 41 (3): 030001. Bibcode:2017ChPhC..41c0001A. doi:10.1088/1674-1137/41/3/030001.
- ^ Davy, H. (1808) "Electro-chemical researches on the decomposition of the earths; with observations on the metals obtained from the alkaline earths, and on the amalgam procured from ammonia," Philosophical Transactions of the Royal Society of London, vol. 98, pp. 333–370.
- ^ Krebs, Robert E. The history and use of our earth's chemical elements: a reference guide. Greenwood Publishing Group. 2006: 80. ISBN 0-313-33438-2.
- ^ Masthead. Annalen der Chemie und Pharmacie. 1855, 93 (3): fmi–fmi. doi:10.1002/jlac.18550930301.
- ^ Wagner, Rud; Neubauer, C.; Deville, H. Sainte-Claire; Sorel; Wagenmann, L.; Techniker; Girard, Aimé. Notizen. Journal für Praktische Chemie. 1856, 67: 490–508. doi:10.1002/prac.18560670194.
- ^ Jensen, William B. The Origin of the Brin Process for the Manufacture of Oxygen. Journal of Chemical Education. 2009, 86 (11): 1266. Bibcode:2009JChEd..86.1266J. doi:10.1021/ed086p1266.
- ^ Ihde, Aaron John. The development of modern chemistry. 1984-04-01: 681. ISBN 978-0-486-64235-2.
- ^ Schott, G. D. Some Observations on the History of the Use of Barium Salts in Medicine. Med. Hist. 1974, 18 (1): 9–21. PMC 1081520
 . PMID 4618587. doi:10.1017/S0025727300019190.
. PMID 4618587. doi:10.1017/S0025727300019190.
- ^ M. Michael Miller. Mineral Commodity Summaries, January 2012 - BARITE (PDF). U.S. Geological Survey. [2018-08-10]. (原始内容 (PDF)存档于2018-07-01).
- ^ Jones, Chris J. & Thornback, John. Medicinal applications of coordination chemistry. Royal Society of Chemistry. 2007: 102. ISBN 0-85404-596-1.
- ^ Russell, Michael S. & Svrcula, Kurt. Chemistry of Fireworks. Royal Society of Chemistry. 2008: 110. ISBN 0-85404-127-3.
- ^ Brent, G. F.; Harding, M. D. Surfactant coatings for the stabilization of barium peroxide and lead dioxide in pyrotechnic compositions. Propellants, Explosives, Pyrotechnics. 1995, 20 (6): 300. doi:10.1002/prep.19950200604.
- ^ Wadhawan, Vinod K. Introduction to ferroic materials. CRC Press. 2000: 740. ISBN 978-90-5699-286-6.
- ^ Crystran Ltd. Optical Component Materials. crystran.co.uk. Crystran Ltd. [2018-08-10]. (原始内容存档于2018-07-28).
- ^ Wu, M.; Ashburn, J.; Torng, C.; Hor, P.; Meng, R.; Gao, L.; Huang, Z.; Wang, Y.; Chu, C. Superconductivity at 93 K in a New Mixed-Phase Y-Ba-Cu-O Compound System at Ambient Pressure. Physical Review Letters. 1987, 58 (9): 908–910. Bibcode:1987PhRvL..58..908W. PMID 10035069. doi:10.1103/PhysRevLett.58.908.
- ^ 22.0 22.1 22.2 22.3 22.4 Barium. ESPI Metals. [2012-06-11].
- ^ Patnaik, Pradyot. Handbook of inorganic chemicals. 2003: 77–78. ISBN 0-07-049439-8.
- ^ Toxicity Profiles, Ecological Risk Assessment. US EPA. [2012-06-16]. (原始内容存档于2010-01-10).
- ^ Moore, J. W. Inorganic Contaminants of Surface Waters, Research and Monitoring Priorities. New York: Springer-Verlag. 1991.
- ^ Doig, A.T. Baritosis: a benign pneumoconiosis. Thorax. 1976, 31 (1): 30–9. PMC 470358
 . PMID 1257935. doi:10.1136/thx.31.1.30.
. PMID 1257935. doi:10.1136/thx.31.1.30.
- 元素钡在洛斯阿拉莫斯国家实验室的介绍(英文)
- EnvironmentalChemistry.com —— 钡(英文)
- 元素钡在The Periodic Table of Videos(诺丁汉大学)的介绍(英文)
- 元素钡在Peter van der Krogt elements site的介绍(英文)
- WebElements.com – 钡(英文)

