

| 此条目没有列出任何参考或来源。 (2019年7月22日) 维基百科所有的内容都应该可供查证。请协助补充可靠来源以改善这篇条目。无法查证的内容可能会因为异议提出而移除。 |
硫(拼音:liú,注音:ㄌ丨ㄡˊ,粤拼:lau4;英语:Sulfur),是一种化学元素,其化学符号为S,原子序数为16,原子量为32.066 u。硫是一种非常常见的无味无臭的非金属,纯的硫是黄色的晶体,又称硫黄、硫磺。硫有许多不同的化合价,常见的有-2, 0, +4, +6等。在自然界中常以硫化物或硫酸盐的形式出现,尤其在火山地区纯的硫也在自然界出现。硫单质难溶于水,微溶于乙醇,易溶于二硫化碳。对所有的生物来说,硫都是一种重要的必不可少的元素,它是多种氨基酸的组成部分,尤其是大多数蛋白质的组成部分。它主要被用在肥料中,也广泛地被用在火药、润滑剂、杀虫剂和抗真菌剂中。
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 外观 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
黄色晶体 硫的原子光谱 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 概况 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 名称·符号·序数 | 硫(Sulfur)·S·16 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 元素类别 | 非金属、氧族元素 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 族·周期·区 | 16 ·3·p | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 标准原子质量 | 32.066(4) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 电子排布 | [Ne] 3s2 3p4 2, 8, 6  | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 历史 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 确认其为一元素者 | 安托万-洛朗·德·拉瓦锡 (1777) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 物理性质 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 物态 | 固体 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 | (接近室温) (斜方硫) 2.07 g·cm−3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 | (接近室温) (单斜硫) 1.96 g·cm−3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 熔点时液体密度 | 1.819 g·cm−3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 熔点 | 388.36 K,115.21 °C,239.38 °F | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 沸点 | 717.8 K,444.6 °C,832.3 °F | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 临界点 | 1314 K,20.7 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 熔化热 | 1.727 kJ·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 汽化热 | 45 kJ·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 比热容 | 22.75 J·mol−1·K−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
蒸气压
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子性质 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 氧化态 | 6, 5, 4, 3, 2, 1, -1, -2 (强酸性) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 电负性 | 2.58(鲍林标度) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 电离能 | 第一:999.6 kJ·mol−1 第二:2252 kJ·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 共价半径 | 105±3 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 范德华半径 | 180 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 杂项 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 晶体结构 | 正交 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 磁序 | 抗磁性[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 磁化率 | (α) −15.5·10−6 (298 K)[2] cm3/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 电阻率 | (20 °C)(无定形硫) 2×1015 Ω·m | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 热导率 | (无定形硫) 0.205 W·m−1·K−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 体积模量 | 7.7 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 莫氏硬度 | 2.0 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS号 | 7704-34-9 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 最稳定同位素 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
主条目:硫的同位素
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
纯的硫呈浅黄色,质地柔软,轻。与氢结成有毒化合物硫化氢后有一股臭味(臭鸡蛋味)[注 1]。硫燃烧时的火焰是蓝色的,并散发出一种特别的硫磺味(二氧化硫的气味)。硫不溶于水但溶于二硫化碳。硫最常见的化学价是-2、+2、+4和+6。在所有的物态中(固态、液态和气态),硫都有不同的同素异形体,这些同素异形体的相互关系还没有被完全理解。晶体的硫可以组成一个由八个原子组成的环:S8。
硫有两种晶体形式:斜方晶八面体和单斜棱晶体,前者在室温下比较稳定。
硫在工业中很重要,比如作为电池中或溶液中的硫酸。硫被用来制造黑火药。在橡胶工业中做硫化剂。硫还被用来杀真菌,用做化肥。硫化物在造纸业中用来漂白。硫酸盐在烟火中也有用途。硫代硫酸钠和硫代硫酸铵在照相中做定影剂。硫酸镁可用做润滑剂,被加在肥皂中和轻柔磨砂膏中,也可以用做肥料。
半胱氨酸、蛋氨酸、同型半胱氨酸和牛磺酸等氨基酸和一些常见的酶含硫,因此硫是所有细胞中必不可少的一种元素。在蛋白质中,多肽之间的二硫键是蛋白质构造中的重要组成部分。有些细菌在一些类似光合作用的过程中使用硫化氢作为电子提供物(一般植物使用水来做这个作用)。植物以硫酸盐的形式吸收硫。无机的硫是铁硫蛋白的一个组成部分。在细胞色素氧化酶中,硫是一个关键的组成部分。
工业和发电厂燃烧煤释放出来的大量二氧化硫在空气中与水和氧结合形成硫酸,它造成酸雨降低水和土壤的pH值,对许多地区的自然环境造成巨大破坏。
在古代人类就已经认识硫了。中国人发明的火药是硝酸钾、碳和硫的混合物。1770年代安托万·拉瓦锡证明硫是一种元素。


在自然界中硫主要以硫化物(如黄铁矿)和硫酸盐(如石膏)的形式出现,在热泉和火山地区也有纯的硫存在。除此以外一些矿物如辰砂、方铅矿、闪锌矿和辉锑矿等也都是硫化物的矿物。煤和石油中也含少量硫,这是为什么在燃煤和石油时有二氧化硫被释放出来(酸雨)。今天许多国家要求燃烧煤和石油时被释放的二氧化硫要进行回收。这些被回收的硫是今天工业中使用的硫的一个重要来源。此过程通常通过一个叫做“克劳斯工艺”的过程来实现。另一个重要来源是硫矿。
在工业中,最重要的硫的化合物是硫酸。硫酸是所有工业过程中必不可少的一个原材料,因此硫酸的消耗量被看做是一个国家工业化程度的一个指标。在美国硫酸是所有生产得最多的化合物。
木卫一表面的黄色主要是它的火山释放的硫造成的。月球上阿利斯塔克环形山中比较暗的地区可能是硫形成的。在许多陨石中有硫。基于人类对外星资源的兴趣强烈提升,木卫一的硫磺也曾经是研究考虑开采的对象;然而成本惊人,除了构想以外,并未付诸实行。
许多有机物难闻的味道来自于它们分解产生的硫化氢之类的化合物。这些化合物有一股特别的臭鸡蛋味道。硫化氢的溶液是酸性的,与金属反应形成金属的硫化物。铁的硫化物在大自然中很常见,如黄铁矿。黄铁矿有半导体的特性。方铅矿即硫化铅则是第一种被发现的半导体。
聚合的氮化硫有金属特性,尽管它不含任何金属,这个复合物还显示特别的电学和光学特性。让熔化的硫速凝可以获得无晶态的硫,伦琴衍射显示其中含有由八个硫原子组成的环。这种硫在室温下不十分稳定,它渐渐恢复为晶体状态。
硫有多种氧化物,除了


其它重要的硫的化合物有:
- 连二亚硫酸钠:
,是一种强有力的还原剂
- 亚硫酸:
,是二氧化硫在水中的溶液。亚硫酸和亚硫酸盐是有力的还原剂 。二氧化硫的其它产物包括焦亚硫酸离子(
)
- 硫代硫酸盐:
,是氧化剂。硫代硫酸氨有可能可以代替氰化物来洗金
- 连二硫酸:
,及其盐
- 连多硫酸:
,n可以从3一直到80
- 硫酸盐:是硫酸的盐
- 硫化物:是硫与其它元素的化合物
- 过一硫酸是三氧化硫与浓的过氧化氢的反应物
- 硫氰酸盐是硫氰离子(
)的化合物
- 硫氰:
- 二硫化碳:一种良好的有机溶剂,通常用于纺织工业,工业上通过甲烷与硫磺反应来生产
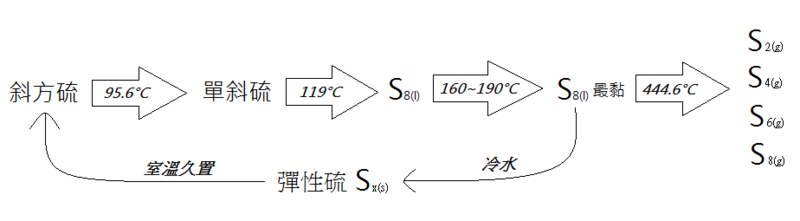
- 斜方硫(菱形硫): Dolomite Rhombic sulfur
- 化学式:
- 是硫由二硫化碳结晶而得之紧密的黄色晶体,熔点112.8度。
- 化学式:
- 单斜硫:Monoclinic sulfur
- 化学式:
- 熔化硫于部分凝固后,倒出多余液体,剩下无数之针形晶体即为单斜硫,熔点119.2度。
- 化学式:
- 弹性硫: Plastic sulfur
- 化学式:
- 为沸腾之硫注入冷水所得之软黏体,有弹性。
- 化学式:
硫有18种同位素,其中四种是稳定的:S-32(95.02%)、S-33(0.75%)、S-34(4.21%)和S-36(0.02%),除
硫化物沉淀时根据温度的不同S-34的含量少许不同。假如在一个矿物中硫化物和碳酸盐同时存在的话,那么根据碳-13和硫-34的含量可以推算出矿物形成时矿水的pH值和氧的逸度。
在森林生态系统中,硫酸盐主要来自空气,少量来自矿物的风化。其中硫的同位素的不同含量可用来确定它们的来历。
在接触二硫化碳、硫化氢和二氧化硫时要非常小心。二氧化硫可以在肺中与水结合成亚硫酸,亚硫酸可以导致肺出血和窒息。硫化氢毒性非常高。虽然硫化氢的味道一开始非常强烈,但人的嗅觉很快就被它压抑了。因此受害人有可能未察觉它的存在。
- ^ 一般所谓硫的臭味其实是硫化氢或是有机硫化合物的臭味
- ^ Lide, D. R. (编). Magnetic susceptibility of the elements and inorganic compounds. CRC Handbook of Chemistry and Physics (PDF) 86th. Boca Raton (FL): CRC Press. 2005. ISBN 0-8493-0486-5.
- ^ Weast, Robert. CRC, Handbook of Chemistry and Physics. Boca Raton, Florida: Chemical Rubber Company Publishing. 1984: E110. ISBN 0-8493-0464-4.
- 刘广定:〈中国用硫史研究:古代纯化硫磺法初探 (页面存档备份,存于互联网档案馆)〉。
- Taeheon Lee, Philip T. Dirlam, Jon T. Njardarson, Richard S. Glass, Jeffrey Pyun. Polymerizations with Elemental Sulfur: From Petroleum Refining to Polymeric Materials. Journal of the American Chemical Society. 2022-01-12, 144 (1): 5–22 [2022-02-15]. ISSN 0002-7863. doi:10.1021/jacs.1c09329. (原始内容存档于2022-02-20) (英语).
- 元素硫在洛斯阿拉莫斯国家实验室的介绍(英文)
- EnvironmentalChemistry.com —— 硫(英文)
- 元素硫在The Periodic Table of Videos(诺丁汉大学)的介绍(英文)
- 元素硫在Peter van der Krogt elements site的介绍(英文)
- WebElements.com – 硫(英文)


