Uue(英语:Ununennium,化学符号为Uue)是一种尚未被发现的化学元素,原子序数是119。直到这个元素被发现、确认并确定了永久名称之前,Ununennium和Uue分别为这个元素的暂时系统命名和化学符号。在元素周期表里,Uue预测是s区元素和碱金属,也是第一个第8周期元素。它是目前最轻的未发现元素。
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 概况 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 名称·符号·序数 | Ununennium·Uue·119 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 元素类别 | 未知 可能为碱金属 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 族·周期·区 | 1 ·8·s | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 标准原子质量 | [315](预测)[1] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 电子排布 | [Og] 8s1(预测[2]) 2, 8, 18, 32, 32, 18, 8, 1(预测)  | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 物理性质 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 物态 | 液体(有可能为固体)[2] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 | (接近室温) 3(预测)[2] g·cm−3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 熔点 | 273–303 K,0–30 °C,32–86(预测)[2] °F | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 沸点 | 903 K,630 °C,1166(预测)[1] °F | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 熔化热 | 2.01–2.05(外推)[3] kJ·mol−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 蒸气压 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子性质 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 氧化态 | 1, 3(预测)[2] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 电负性 | 0.86(预测)[4](鲍林标度) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 电离能 | 第一:463.1 kJ·mol−1 第二:1698.1(预测)[5] kJ·mol−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子半径 | 240(预测)[2] pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 共价半径 | 263-281(外推)[3] pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 晶体结构 | 面心立方晶系(外推)[6] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
日本的理化学研究所正在尝试合成该元素,俄罗斯杜布纳联合原子核研究所也在计划合成。理论和实验证据表明,Uue的合成很可能比之前的元素要困难得多,甚至可能是目前技术可以合成的倒数第二个元素。
Uue在第七种碱金属的位置表明它会和较轻的同类物有相似的性质。不过,相对论效应可能会导致Uue的某些性质与直接用元素周期律推测的性质不同。举个例子,Uue预测会比铯和钫更不活泼,反应性更像钾或铷。Uue会有碱金属特征性的+1氧化态,但预测也有其它碱金属都未知的+3氧化态。
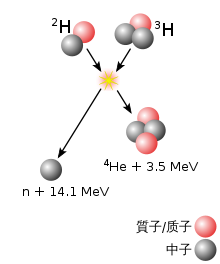
| 外部视频链接 | |
|---|---|
超重元素[a]的原子核是在两个不同大小的原子核[b]的聚变中产生的。粗略地说,两个原子核的质量之差越大,两者发生反应的可能性就越大。[13]由较重原子核组成的物质会作为靶子,被较轻原子核的粒子束轰击。两个原子核只能在距离足够近的时候,才能聚变成一个原子核。原子核(全部都有正电荷)会因为静电排斥而相互排斥,所以只有两个原子核的距离足够短时,强核力才能克服这个排斥力并发生聚变。粒子束因此被粒子加速器大大加速,以使这种排斥力与粒子束的速度相比变得微不足道。[14]不过,只是靠得足够近不足以使两个原子核聚变:当两个原子核逼近彼此时,它们通常会在一起约10−20秒后裂变(产物不需要和反应物相同),而非形成单独的原子核。[14][15]如果聚变发生了,两个原子核产生的一个原子核会处于激发态[16],被称为复合原子核,非常不稳定。[14]为了达到更稳定的状态,这个暂时存在的原子核可能会直接核裂变,[17]或是放出一些带走激发能量的中子。如果这些激发能量不足以使中子被放出,复合原子核就会放出γ射线。这个过程会在原子核碰撞后的10−16秒发生,并创造出更稳定的原子核。[17]联合工作团队(JWP)定义,化学元素的原子核只有10−14秒内不进行放射性衰变,才能被识别出来,这个值大约是原子核得到它的外层电子,显示其化学性质所需的时间。[18][c]
粒子束穿过目标后,会到达下一个腔室——分离室。如果反应产生了新的原子核,它就会被这个粒子束携带。[20]在分离室中,新产生的原子核会从其它核素(原本的粒子束和其它反应产物)中分离,[d]并转移到半导体探测器中,在这里停止原子核。这时标记撞击探测器的确切位置、能量和到达时间。[20]这个转移需要10−6秒的时间,意即这个原子核需要存活这么长的时间才能被检测到。[23]衰变被记录后,这个原子核被再次记录,并测量位置、衰变能量和衰变时间。[20]
原子核的稳定性源自于强核力,但强核力的作用距离很短,随着原子核越来越大,强核力对最外层的核子(质子和中子)的影响减弱。同时,原子核会被质子之间,范围不受限制的静电排斥力撕裂。[24]超重元素[25]的主要衰变方式——α衰变和自发裂变都是这种排斥引起的。[e]α衰变由发射出去的α粒子记录,在实际衰变之前很容易确定衰变产物。如果这样的衰变或一系列连续衰变产生了一个已知的原子核,则可以很容易地确定反应的原始产物。[f](衰变链中的所有衰变都必须在同一个地方发生。)[20] 已知的原子核可以通过它经历的衰变的特定特征来识别,例如衰变能量(或更具体地说,发射粒子的动能)。[g]然而,自发裂变会产生各种分裂产物,因此无法从其分裂产物确定原始核素。[h]
尝试合成超重元素的物理学家可以获得的信息是探测器收集到的信息:粒子到达探测器的位置、能量和时间,以及粒子衰变的信息。物理学家分析这些数据并试图得出结论,确认它确实是由新元素引起的,而非由不同的核素引起的。如果提供的数据不足以得出创造出来的核素确实是新元素的结论,并且对观察到的影响没有其他解释,就可能在解释数据时出现错误。[i]
超重元素是通过核聚变产生的。根据产物复合原子核的激发能量,这些核聚变反应可以分为热核聚变和冷核聚变。[j]在热核聚变中,非常轻、高能量的发射体加速砸向非常重的目标(锕系元素),产生的复合原子核有高激发能量(~40–50 MeV)。它们可能会直接裂变,或是放出多颗(3到5)中子。[38]在冷核聚变反应中,会使用更重的第4周期元素发射体,以及较轻的铅和铋目标。产生的复合原子核的激发能量相对较低(~10–20 MeV),减少了直接裂变的可能性。当产生的复合原子核回到基态后,它们只需要发射一到两颗中子。不过,热核聚变反应可以产生有更多中子的产物,因为锕系元素在所有可以大量制造的元素中有最高的中子/质子比。[39]
Uue和Ubn(元素119和120)都是还没被发现的元素中,原子序最低的。由于反应的截面减少,半衰期也可能很短(微秒级别[2][40]),尝试合成它们将突破当前技术的极限。[41]Ubu(元素121)之后的元素因为半衰期太短,会在到达探测器之前的一微秒内衰变,所以当前技术可能无法检测到它们。检测到元素121到124的可能性在很大程度上取决于所使用的理论模型,因为它们的半衰期预计非常接近一微秒。[41]此前,超重元素合成中的重要帮助来自𬭶-270周围变形的核壳层,增加了周围核素的稳定性。此外,接近稳定的富中子同位素钙-48可用作发射体,产生更多超重元素的富中子同位素。[42]超重元素原子核的中子越多,它就预计越接近稳定岛。[k]即便如此,合成出来的同位素的中子数仍然比稳定岛中预期的要少。[45]此外,使用钙-48发射体来合成Uue需要锿做的目标,后者难以大量制备(只能合成微克级别,而锫和锎可以做到毫克级别),所以更重的超重元素更实际的合成方法将会需要比48Ca重的发射体。[42]
尝试合成
1985年,人们在加州伯克利的superHILAC加速器通过用钙-48离子轰击锿-254,首次尝试合成Uue:
反应没有检测到任何原子,截面上限为300 nb。[46]之后的计算认为3n反应(产物为299Uue和三个中子)的截面实际上少了六十万倍,为0.5 pb。[47]
1999年,劳伦斯伯克利国家实验室通过208Pb和86Kr的反应,声称合成了293Og。因此,类似的反应209Bi + 86Kr和208Pb + 87Rb被提议用于合成元素119和它未知的α衰变产物——元素117、115和113。[48]2001年这些结果的撤回[49]和最近对冷聚变反应截面的计算对这种可能性提出了质疑。举个例子,209Bi + 86Kr反应的横截面上限预测为2 fb。[50]放射性的发射体可以提供利用铅或铋目标的替代方法,可以产生更多富中子的同位素。[50]
从2012年4月到9月,在德国达姆施塔特亥姆霍兹重离子研究中心通过用钛-50轰击锫-249,尝试合成295Uue和296Uue。[51][52]249Bk和50Ti的反应被预测为实际上制备Uue最有利的反应,[52]因为反应比较不对称,[41]尽管反应有点冷。[53]254Es和48Ca的反应更好,但是制备毫克量级的254Es来作为目标很难。[41]而且,锫-249会衰变成下一个元素锎-249,半衰期只有短短的327天,所以可以同时寻找元素119和120。[54]然而,由于发射体从48Ca改成了50Ti,Uue的预期产量将除以二十倍,因为产量在很大程度上取决于聚变反应的不对称性。[41]由于预计Uue的半衰期较短,GSI团队使用了能够在微秒内记录衰变事件的新型快速电子设备。[52][41]
元素119和元素120都没有被发现,这意味着在这些反应中生成元素119的限制截面为65 fb,而生成元素120的限制截面为200 fb。[53][54]在该反应中生产元素119的预测实际横截面约为40 fb,是当前技术的极限。[41](记录中有最低截面的成功反应是209Bi和70Zn反应产生鿭的反应,为30 fb。)[41]这个实验原本会持续到2012年11月,[55]但实验人员把发射体改成48Ca以确认鿬的发现,提早结束实验。[53]
位于日本埼玉县和光市的理化学研究所团队在2018年6月开始用钒-51轰击锔-248目标来合成Uue。[56]由于较重的锫或锎难以制备,他们选择了锔来作为目标。[57]由于反应的不对称性降低,预计的截面大约减半,需要至少30 fb的灵敏度。[54]这些248Cm目标由橡树岭国家实验室提供,他们也为鿬(元素117)的合成中提供了249Bk目标。实验开始于回旋加速器,而理化学研究所于2020年升级了它的直线加速器。[58]两台机器都可以继续轰击,直到观察到第一个事件,该实验目前是间歇性运行,每年至少进行100天。[56][57]理化学研究所仁科中心主任延与秀人预测,到2022年时可能会发现元素119和120。[59]理化学研究所团队的尝试会由天皇资助。[60]
产生的Uue同位素预计会进行两次α衰变,产生镆的已知同位素(288Mc和287Mc)。在这之后已知会发生五个α衰变事件,就可以证实它们的发现。这些反应的预测截面约为10 fb。[57]
俄罗斯杜布纳联合原子核研究所的团队计划开始使用249Bk + 50Ti反应来合成Uue。[61][62][63][64][65][66]
日本的理化学研究所和俄罗斯的JINR实验室最适合这些实验,因为它们是世界上唯一可以进行低截面反应的实验室。[67]
命名
根据门捷列夫对未发现元素的命名方法,Uue可称为eka-钫。1979年,IUPAC发布了有关新元素命名的建议,根据这一规则119号元素应称为ununennium,化学符号Uue。[68]尽管这在化学界的各个层面,从化学课堂到高级教科书都在广泛使用,但在超重元素理论或实验上工作的科学家中,这些建议大多被忽视,并将这个元素称之为“元素119”,化学符号E119、(119)或119。[2]
核稳定性和同位素
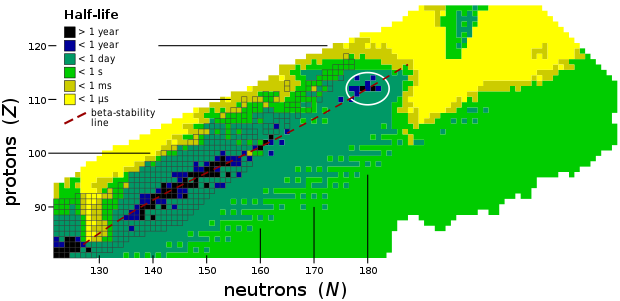
原子核的稳定性在锔(元素96)之后迅速下降,它的半衰期比其它原子序更高的元素高了四个数量级。钔(元素101)之后的元素的半衰期都少于30个小时。在铅(元素82)之后的元素都没有稳定同位素。[69]尽管如此,由于尚未完全了解的原因,在原子序110至114周围的原子核的稳定性略微增加,这导致了核物理学中所谓的“稳定岛”的出现。加利福尼亚大学伯克利分校的格伦·西奥多·西博格教授提出的这个概念解释了为什么超重元素的半衰期比预测的要长。[70]
291–307Uue预测的α衰变半衰期都是微秒级别的,其中294Uue的α衰变半衰期最长,预测约485微秒。[71][72][73]不过如果算上所有的衰变方式,它们的半衰期预测只剩几十微秒。[2][40]更重的同位素应该会更稳定。1971年,Fricke和Waber预测315Uue是Uue最稳定的同位素。[1]这会对Uue的合成产生影响,因为半衰期低于一微秒的同位素会在到达探测器之前衰变,而较重的同位素无法通过任何已知可用目标和发射体的碰撞来合成。[2][40]然而,新的理论模型表明,质子轨道2f7/2(会在元素114填充)和2f5/2(会在元素120填充)之间的能量差距比预期的要小,使得元素114不再是稳定的球形封闭原子核,而这个能隙可能会增加元素119和120的稳定性。下一个有双幻数的原子核预计在306Ubb(元素122)周围,但是该核素预期的低半衰期和低截面使其合成具有挑战性。[74]
原子和物理性质
作为第一个第8周期元素,Uue预测是碱金属,在元素周期表中的位置在锂、钠、钾、铷、铯和钫之下。这些元素在最外层的s轨道中都有一个价电子(价电子排布ns1),这个电子在化学反应中可以轻易失去,形成+1氧化态。因此,碱金属是反应性很高的元素。Uue预计会延续这个趋势,价电子的排布为8s1。因此,人们预计Uue的行为很像它的较轻的同类物。然而据预测,它在某些特性上与较轻的碱金属不同。[2]
Uue和其它碱金属有不同之处的主要原因是自旋-轨道作用——电子运动与自旋之间的相互作用。自旋-轨道作用对于超重元素尤其强烈,因为它们的电子比轻原子中的电子移动得更快,速度与光速相当。[75]在Uue原子中,7p和8s电子能级下降,对应的电子变得稳定,但有两个7p电子能级要比其它四个更稳定。[76]这个效应被称为亚层分裂,因为它将7p亚层分裂成更稳定和更不稳定的部分。计算化学家将这种分裂理解为角量子数 l 从1分裂成1/2和3/2,分别为7p亚层较稳定和较不稳定的部分。[75][l]因此,Uue外层的8s电子变得稳定,会比预期更难移除,而7p3/2电子则变得不稳定,可能允许它们参与化学反应。[2]最外层s轨道(在钫中就已经很重要)的这种稳定性是影响Uue的化学性质的关键因素,并会导致碱金属的原子和分子性质的所有趋势在铯之后反转。[4]
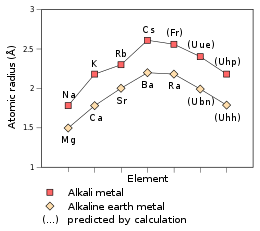 从第3至第9周期的碱金属和碱土金属的原子半径的实测值(Na–Cs,Mg–Ra)和预测值(Fr–Uhp,Ubn–Uhh),单位为埃格斯特朗。[2][77] |
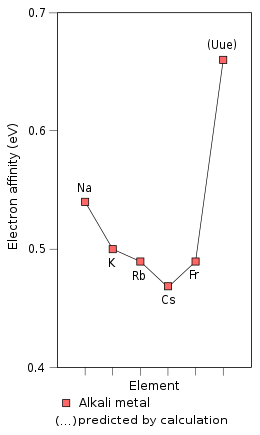 从第3到第8周期的碱金属的电子亲和能的实测值(Na–Cs)、半实测值(Fr)和预测值(Uue),单位为电子伏特。[2][77]电子亲和能从Li到Cs一直下降,但Fr的492±10 meV比Cs的电子亲和能高了20 meV,而Uue的电子亲和能更高,达到662 meV。[78] |
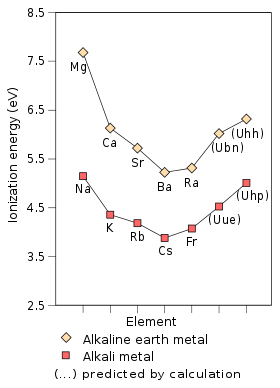 从第3到第9周期的碱金属和碱土金属的第一电离能的实测值(Na–Fr,Mg–Ra)和预测值(Uue–Uhp,Ubn–Uhh),单位为电子伏特。[2][77] |
由于外层的8s电子变得稳定,Uue的第一电离能(从电中性原子中移除一个电子所需的能量)预测为4.53 eV,比钾之后的所有碱金属都高。这个影响是如此的大,使得Ubu(元素121)预测有比Uue更低的电离能,为4.45 eV。因此,第8周期的碱金属Uue不是整个周期电离能最低的,这和之前的所有周期不同。[2]Uue的电子亲和能预计远大于铯和钫。它的电子亲和能比所有更轻的碱金属都高,为0.662 eV,接近于钴(0.662 eV)和铬(0.676 eV)。[78]相对论效应也会导致Uue的极化性大幅下降[2]到169.7 a.u.。[79]事实上,计算出来的Uue的静态偶极极化性(αD)很小,接近于钠。[80]
Uue的类氢原子(只有一个电子的原子)——Uue118+的电子预测会非常快地移动,使得它的质量是静止电子的1.99倍,是相对论效应的特征。作为比较,钫的类氢原子的电子质量为1.29,铯的则为1.091。[75]根据相对论的简单外推,这间接表明了Uue的原子半径会收缩[75]到只有240 pm,[2]很接近铷的247 pm,而Uue的金属半径也相应降低到260 pm。[2]Uue+的离子半径预测为180 pm。[2]
Uue的熔点预测在0℃和30℃之间,所以在室温下可能是液体。[5]人们还不知道这是否符合熔点继续降低的趋势,因为铯的熔点为28.5℃,而钫的熔点估计约为8.0℃。[81]Uue的沸点预测在630℃左右,类似钫的620℃左右,它们都比铯的671℃低。[1][81]Uue的密度预计在3到4 g/cm3之间,符合随着族往下密度一直增加的趋势:钫的密度预测为2.48 g/cm3,而铯的密度是1.93 g/cm3。[1][3][81]
化学性质
| 化合物 | 键长(Å) | 键解离能(kJ/mol) |
|---|---|---|
| Li2 | 2.673 | 101.9 |
| Na2 | 3.079 | 72.04 |
| K2 | 3.924 | 53.25 |
| Rb2 | 4.210 | 47.77 |
| Cs2 | 4.648 | 43.66 |
| Fr2 | ~4.61 | ~42.1 |
| Uue2 | ~4.27 | ~53.4 |
Uue的化学性质预测类似碱金属,[2]但它的性质比起铯或钫,会更像钾[83]或铷[2]。这是由于相对论效应导致的,如果不存在相对论效应,元素周期律将预测Uue比铯和钫更具反应性。由于相对论效应稳定了它的价电子,增加了第一电离能,使得Uue的反应性、金属半径和离子半径降低了。[83]这个效应在钫中就已经出现了。[2]
+1氧化态的Uue的化学性质比起钫会更像铷。另一方面,由于变得不稳定而比其它p轨道大的7p轨道,Uue+的离子半径预测大于Rb+。除了其它碱金属特征性且主要的+1氧化态以外,Uue可能也有在其它碱金属都未发现[84]的+3氧化态。[2]这是因为7p3/2轨道的不稳定和膨胀,导致其电子的电离能低于预期。[2][84]由于成键时也涉及了7p3/2电子,很多Uue的化合物都预计有很大的共价性。这个效应也在钫中出现,其中超氧化钫(FrO2)的成键中有一些6p3/2的成分。[75]因此,Uue不能替代铯,成为电正性最高的元素,而它的电负性最有可能接近钠的0.93(鲍林标度)。[4]Uue+/Uue的标准电极电势预测为−2.9 V,和Fr+/Fr一样只是略微大于K+/K的−2.931 V。[5]
在气相中以及在非常低温下的凝聚相中,碱金属会形成以共价键键合的双原子分子。在这些M2分子里,它们的金属-金属键长从Li2到Cs2一直增加,但由于上述8s轨道的相对论效应,Uue2的键长下降。在这些分子的键解离能中有相反的趋势,其中Uue–Uue键应该比K–K键略强。[4][82]Uue的升华热(ΔHsub)预测为94 kJ/mol(钫的值在77 kJ/mol左右)。[4]
由于Uue的高电子亲和能,UueF分子预计有显著的共价性。UueF中的成键主要是Uue的7p轨道和氟的2p轨道成的键,来自氟的2s轨道和Uue的8s、6dz2和其它两个7p轨道对键的贡献较少。这和其它s区元素、金和汞的行为非常不同,它们使用s轨道(有时混合d轨道)来成键。Uue–F键因为相对论效应把7p轨道分成7p1/2和7p3/2而扩张,这和氢化物AtH和TsH的键扩张类似。[85]Uue–Au键将会是金和碱金属之间最弱的键,但仍然是稳定的。通过外推,可以给出Uue的吸附焓(−ΔHads):在金上为106 kJ/mol(钫的值是136 kJ/mol)、在铂上为76 kJ/mol、在银上为63 kJ/mol,都是碱金属之中最低。这些数据表明,在由贵金属制成的表面上研究Uue的色谱法吸附是可行的。[4]Uue在聚四氟乙烯表面的吸附焓预测为17.6 kJ/mol,是碱金属当中最低的。这些信息对于Uue未来的化学实验非常有用。[79]碱金属的ΔHsub和−ΔHads值都不成比例相关,因为它们会随着原子序数的增加而向相反的方向变化。[4]
- ^ 在核物理学中,如果一个元素有高原子序,就可以被称为重元素。82号元素铅就是重元素的例子。“超重元素”这一词通常指原子序大于103的元素(尽管也有其它的定义,例如原子序大于100[8]或112。[9]有时这一词和锕系后元素是同义词,将超重元素的上限定在还未发现的超锕系元素的开始。)[10](那个元素的)“超重同位素”和“超重核素”顾名思义——分别是(那个元素的)高质量同位素和高质量的核素。
- ^ 2009年,由尤里·奥加涅相引领的团队在JINR发表了他们通过对称的136Xe + 136Xe反应,尝试合成钅黑的结果。他们未能在这个反应中观察到单个原子,因此对截面设置了上限,即核反应概率的度量为2.5 pb。[11]作为比较,发现钅黑的反应208Pb + 58Fe的截面约为20 pb(进一步来说,为19+19-11 pb),符合发现者的预测。[12]
- ^ 这个值也标志着普遍接受的复合原子核寿命上限。[19]
- ^ 这种分离是基于产生的原子核会比未反应的粒子束更慢地通过目标。分离器中包含电场和磁场,它们对运动粒子的影响会因粒子的特定速度而被抵消。[21]飞行时间质谱法和反冲能量的测量也有助于这种分离,两者结合可以估计原子核的质量。[22]
- ^ 不是所有放射性衰变都是因为静电排斥力导致的。举个例子,β衰变是弱核力导致的。[26]
- ^ 由于原子核的质量不是直接测量的,而是根据另一个原子核的质量计算得出的,因此这种测量称为间接测量。直接测量也是有可能的,但在大多数情况下,它们仍然无法用于超重原子核。[27]2018年,LBNL首次直接测量了超重原子核的质量,[28]它的质量是根据转移后原子核的位置确定的(位置有助于确定其轨迹,这与原子核的质荷比有关,因为转移是在有磁铁的情况下完成的)。[29]
- ^ 如果在真空中发生衰变,那么由于孤立系统在衰变前后的总动量必须保持守恒,衰变产物也将获得很小的速度。这两个速度的比值以及相应的动能比值与两个质量的比值成反比。衰变能量等于α粒子和衰变产物的已知动能之和。[30]这些计算也适用于实验,但不同之处在于原子核在衰变后不会移动,因为它与探测器相连。
- ^ 自发裂变是由苏联科学家格奥尔基·弗廖罗夫发现的。[31]LBL的科学家们认为自发裂变的信息不足以声称合成元素,他们认为对自发裂变的研究还不够充分,无法将其用于识别新元素,因为很难确定复合原子核是不是仅喷射中子,而不是质子或α粒子等带电粒子。[19]因此他们更喜欢通过连续的α衰变将新的同位素与已知的同位素联系起来。[31]
- ^ 举个例子,1957年,元素102在瑞典斯德哥尔摩省斯德哥尔摩的诺贝尔物理研究所被错误地鉴定。[32]早先没有关于该元素发现的明确声明,所以由它的瑞典、美国和英国发现者命名为nobelium。后来证明这个元素的鉴定是错误的。[33]第二年,RL无法重现瑞典的结果,而是宣布他们合成了该元素,这一说法后来也被驳回。[33] JINR坚持认为他们是第一个发现该元素的人,并为新元素建议命名为joliotium,[34]而这个名称也没有被接受(JINR后来认为元素102的命名是仓促的)。[35]这个名称是在IUPAC对元素发现优先权的裁决的书面答复中提出的,该裁决于1992年9月29日签署。[35]但由于其广泛使用,“nobelium”这个名称仍然保持不变。[36]
- ^ 虽然叫做“冷核聚变”,但在超重元素合成中的“冷核聚变”和可以在室温条件下实现核聚变不是一个相同的概念(见冷核聚变)。[37]
- ^ 轻元素的稳定同位素的中子/质子比通常等于或接近一(举个例子,铝唯一的稳定同位素有13个质子和14个中子,[43]中子/质子比为1.077)。不过,较重的元素会有更高的中子/质子比,而且随着质子的增加,这个比例会越来越高(碘唯一的稳定同位素有53个质子和74个中子,中子/质子比为1.396;金唯一的稳定同位素有79个质子和118个中子,中子/质子比为1.494;钚最稳定的同位素有94个质子和150个中子,中子/质子比为1.596)。[43]超重元素预计会延续这个趋势,[44]使得最稳定同位素难以制备,因为产生的原子核的中子/质子比会低于预计的最稳定同位素的低。
- ^ 量子数对应于电子轨道名称中的字母:0为s、1为p、2为d等。更多信息请参见角量子数。
- ^ 1.0 1.1 1.2 1.3 1.4 Fricke, B.; Waber, J. T. Theoretical Predictions of the Chemistry of Superheavy Elements (PDF). Actinides Reviews. 1971, 1: 433–485 [2013-08-07]. (原始内容 (PDF)存档于2016-03-04) (英语).
- ^ 2.00 2.01 2.02 2.03 2.04 2.05 2.06 2.07 2.08 2.09 2.10 2.11 2.12 2.13 2.14 2.15 2.16 2.17 2.18 2.19 2.20 2.21 2.22 2.23 2.24 Hoffman, Darleane C.; Lee, Diana M.; Pershina, Valeria. Transactinides and the future elements. Morss; Edelstein, Norman M.; Fuger, Jean (编). The Chemistry of the Actinide and Transactinide Elements 3rd. Dordrecht, The Netherlands: Springer Science+Business Media. 2006. ISBN 978-1-4020-3555-5 (英语).
- ^ 3.0 3.1 3.2 Bonchev, Danail; Kamenska, Verginia. Predicting the Properties of the 113–120 Transactinide Elements. Journal of Physical Chemistry (American Chemical Society). 1981, 85 (9): 1177–1186 [2021-12-01]. doi:10.1021/j150609a021. (原始内容存档于2015-12-22) (英语).
- ^ 4.0 4.1 4.2 4.3 4.4 4.5 4.6 4.7 Pershina, V.; Borschevsky, A.; Anton, J. Fully relativistic study of intermetallic dimers of group-1 elements K through element 119 and prediction of their adsorption on noble metal surfaces. Chemical Physics (Elsevier). 2012-02-20, 395: 87–94. Bibcode:2012CP....395...87P. doi:10.1016/j.chemphys.2011.04.017 (英语).
这个参考资料给出的马利肯电负性标度是2.72,通过公式χP = 1.35χM1/2 − 1.37转换成鲍林标度 - ^ 5.0 5.1 5.2 Fricke, Burkhard. Superheavy elements: a prediction of their chemical and physical properties. Recent Impact of Physics on Inorganic Chemistry. Structure and Bonding. 1975, 21: 89–144 [4 October 2013]. ISBN 978-3-540-07109-9. doi:10.1007/BFb0116498 (英语).
- ^ Seaborg, Glenn T. Prospects for further considerable extension of the periodic table (PDF). Journal of Chemical Education. 1969, 46 (10): 626–634 [2018-02-22]. Bibcode:1969JChEd..46..626S. doi:10.1021/ed046p626. (原始内容 (PDF)存档于2021-12-09) (英语).
- ^ Wakhle, A.; Simenel, C.; Hinde, D. J.; et al. Simenel, C.; Gomes, P. R. S.; Hinde, D. J.; et al , 编. Comparing Experimental and Theoretical Quasifission Mass Angle Distributions. European Physical Journal Web of Conferences. 2015, 86: 00061. ISSN 2100-014X. doi:10.1051/epjconf/20158600061
 (英语).
(英语).
- ^ Krämer, K. Explainer: superheavy elements. Chemistry World. 2016 [2020-03-15]. (原始内容存档于2021-05-15) (英语).
- ^ Discovery of Elements 113 and 115. Lawrence Livermore National Laboratory. [2020-03-15]. (原始内容存档于2015-09-11) (英语).
- ^ Eliav, E.; Kaldor, U.; Borschevsky, A. Electronic Structure of the Transactinide Atoms. Scott, R. A. (编). Encyclopedia of Inorganic and Bioinorganic Chemistry. John Wiley & Sons: 1–16. 2018. ISBN 978-1-119-95143-8. doi:10.1002/9781119951438.eibc2632 (英语).
- ^ Oganessian, Yu. Ts.; Dmitriev, S. N.; Yeremin, A. V.; et al. Attempt to produce the isotopes of element 108 in the fusion reaction 136Xe + 136Xe. Physical Review C. 2009, 79 (2): 024608. ISSN 0556-2813. doi:10.1103/PhysRevC.79.024608 (英语).
- ^ Münzenberg, G.; Armbruster, P.; Folger, H.; et al. The identification of element 108 (PDF). Zeitschrift für Physik A. 1984, 317 (2): 235–236 [20 October 2012]. Bibcode:1984ZPhyA.317..235M. doi:10.1007/BF01421260. (原始内容 (PDF)存档于7 June 2015) (英语).
- ^ Subramanian, S. Making New Elements Doesn't Pay. Just Ask This Berkeley Scientist. Bloomberg Businessweek. [2020-01-18]. (原始内容存档于2019-12-11) (英语).
- ^ 14.0 14.1 14.2 Ivanov, D. Сверхтяжелые шаги в неизвестное [Superheavy steps into the unknown]. nplus1.ru. 2019 [2020-02-02]. (原始内容存档于2020-04-23) (俄语).
- ^ Hinde, D. Something new and superheavy at the periodic table. The Conversation. 2017 [2020-01-30]. (原始内容存档于2020-03-17) (英语).
- ^ Nuclear Reactions (PDF): 7–8. [2020-01-27]. (原始内容存档 (PDF)于2020-11-30). Published as Loveland, W. D.; Morrissey, D. J.; Seaborg, G. T. Nuclear Reactions. Modern Nuclear Chemistry. John Wiley & Sons, Inc. 2005: 249–297. ISBN 978-0-471-76862-3. doi:10.1002/0471768626.ch10 (英语).
- ^ 17.0 17.1 Krása, A. Neutron Sources for ADS. Faculty of Nuclear Sciences and Physical Engineering (Czech Technical University in Prague). 2010: 4–8. S2CID 28796927 (英语).
- ^ Wapstra, A. H. Criteria that must be satisfied for the discovery of a new chemical element to be recognized (PDF). Pure and Applied Chemistry. 1991, 63 (6): 883 [2021-11-28]. ISSN 1365-3075. doi:10.1351/pac199163060879. (原始内容存档 (PDF)于2021-10-11) (英语).
- ^ 19.0 19.1 Hyde, E. K.; Hoffman, D. C.; Keller, O. L. A History and Analysis of the Discovery of Elements 104 and 105. Radiochimica Acta. 1987, 42 (2): 67–68 [2021-11-28]. ISSN 2193-3405. doi:10.1524/ract.1987.42.2.57. (原始内容存档于2021-11-27) (英语).
- ^ 20.0 20.1 20.2 20.3 Chemistry World. How to Make Superheavy Elements and Finish the Periodic Table [Video]. Scientific American. 2016 [2020-01-27]. (原始内容存档于2020-04-21) (英语).
- ^ Hoffman, Ghiorso & Seaborg 2000,第334页.
- ^ Hoffman, Ghiorso & Seaborg 2000,第335页.
- ^ Zagrebaev, Karpov & Greiner 2013,第3页.
- ^ Beiser 2003,第432页.
- ^ Staszczak, A.; Baran, A.; Nazarewicz, W. Spontaneous fission modes and lifetimes of superheavy elements in the nuclear density functional theory. Physical Review C. 2013, 87 (2): 024320–1. ISSN 0556-2813. doi:10.1103/physrevc.87.024320
 (英语).
(英语).
- ^ Beiser 2003,第439页.
- ^ Oganessian, Yu. Ts.; Rykaczewski, K. P. A beachhead on the island of stability. Physics Today. 2015, 68 (8): 32–38 [2021-11-28]. ISSN 0031-9228. OSTI 1337838. doi:10.1063/PT.3.2880. (原始内容存档于2021-11-28) (英语).
- ^ Grant, A. Weighing the heaviest elements. Physics Today. 2018. doi:10.1063/PT.6.1.20181113a (英语).
- ^ Howes, L. Exploring the superheavy elements at the end of the periodic table. Chemical & Engineering News. 2019 [2020-01-27]. (原始内容存档于2021-11-28) (英语).
- ^ Beiser 2003,第433页.
- ^ 31.0 31.1 Robinson, A. E. The Transfermium Wars: Scientific Brawling and Name-Calling during the Cold War. Distillations. 2019 [2020-02-22]. (原始内容存档于2021-11-28) (英语).
- ^ Nobelium - Element information, properties and uses | Periodic Table. Royal Society of Chemistry. [2020-03-01]. (原始内容存档于2021-03-08) (英语).
- ^ 33.0 33.1 Kragh 2018,第38–39页.
- ^ Kragh 2018,第40页.
- ^ 35.0 35.1 Ghiorso, A.; Seaborg, G. T.; Oganessian, Yu. Ts.; et al. Responses on the report 'Discovery of the Transfermium elements' followed by reply to the responses by Transfermium Working Group (PDF). Pure and Applied Chemistry. 1993, 65 (8): 1815–1824 [7 September 2016]. doi:10.1351/pac199365081815. (原始内容存档 (PDF)于25 November 2013) (英语).
- ^ Commission on Nomenclature of Inorganic Chemistry. Names and symbols of transfermium elements (IUPAC Recommendations 1997) (PDF). Pure and Applied Chemistry. 1997, 69 (12): 2471–2474 [2021-11-28]. doi:10.1351/pac199769122471. (原始内容存档 (PDF)于2021-10-11) (英语).
- ^ Fleischmann, Martin; Pons, Stanley. Electrochemically induced nuclear fusion of deuterium. Journal of Electroanalytical Chemistry and Interfacial Electrochemistry. 1989, 261 (2): 301–308. doi:10.1016/0022-0728(89)80006-3 (英语).
- ^ Barber, Robert C.; Gäggeler, Heinz W.; Karol, Paul J.; Nakahara, Hiromichi; Vardaci, Emanuele; Vogt, Erich. Discovery of the element with atomic number 112 (IUPAC Technical Report). Pure and Applied Chemistry. 2009, 81 (7): 1331. doi:10.1351/PAC-REP-08-03-05
 (英语).
(英语).
- ^ Armbruster, Peter; Munzenberg, Gottfried. Creating superheavy elements. Scientific American. 1989, 34: 36–42.
- ^ 40.0 40.1 40.2 Hofmann, Sigurd. Greiner, Walter , 编. Overview and Perspectives of SHE Research at GSI SHIP. 2013: 23–32 [2021-12-02]. ISBN 978-3-319-00046-6. doi:10.1007/978-3-319-00047-3. (原始内容存档于2021-04-17) (英语).
- ^ 41.0 41.1 41.2 41.3 41.4 41.5 41.6 41.7 41.8 Zagrebaev, Karpov & Greiner 2013.
- ^ 42.0 42.1 Folden III, C. M.; Mayorov, D. A.; Werke, T. A.; Alfonso, M. C.; Bennett, M. E.; DeVanzo, M. J. Prospects for the discovery of the next new element: Influence of projectiles with Z > 20. Journal of Physics: Conference Series. 2013, 420 (1). 012007. Bibcode:2013JPhCS.420a2007F. S2CID 119275964. arXiv:1209.0498
 . doi:10.1088/1742-6596/420/1/012007 (英语).
. doi:10.1088/1742-6596/420/1/012007 (英语).
- ^ 43.0 43.1 Audi, Georges; Bersillon, Olivier; Blachot, Jean; et al. The NUBASE evaluation of nuclear and decay properties (PDF). Nuclear Physics A. 2003, 729 (1): 3–128 [2010-07-05]. Bibcode:2003NuPhA.729....3A. CiteSeerX 10.1.1.692.8504
 . doi:10.1016/j.nuclphysa.2003.11.001. (原始内容 (PDF)存档于2011-07-20) (英语).
. doi:10.1016/j.nuclphysa.2003.11.001. (原始内容 (PDF)存档于2011-07-20) (英语).
- ^ Karpov, A. V.; Zagrebaev, V. I.; Palenzuela, Y. Martinez; Greiner, Walter. Superheavy Nuclei: Decay and Stability. Exciting Interdisciplinary Physics. 2013: 69. ISBN 978-3-319-00046-6. S2CID 55180285. doi:10.1007/978-3-319-00047-3_6 (英语).
- ^ Universal nuclide chart. Nucleonica. Institute for Transuranium Elements. 2007–2012 [2012-07-03]. (原始内容存档于2017-02-19) (英语).

- ^ Lougheed, R.; Landrum, J.; Hulet, E.; et al. Search for superheavy elements using 48Ca + 254Esg reaction. Physical Review C. 1985, 32 (5): 1760–1763. Bibcode:1985PhRvC..32.1760L. PMID 9953034. doi:10.1103/PhysRevC.32.1760 (英语).
- ^ Feng, Z.; Jin, G.; Li, J.; Scheid, W. Production of heavy and superheavy nuclei in massive fusion reactions. Nuclear Physics A. 2009, 816 (1): 33. Bibcode:2009NuPhA.816...33F. S2CID 18647291. arXiv:0803.1117
 . doi:10.1016/j.nuclphysa.2008.11.003 (英语).
. doi:10.1016/j.nuclphysa.2008.11.003 (英语).
- ^ Hoffman, Ghiorso & Seaborg 2000,第431页.
- ^ Public Affairs Department. Results of element 118 experiment retracted. Berkeley Lab. 2001-07-21 [2008-01-18]. (原始内容存档于2008-01-29).
- ^ 50.0 50.1 Loveland, W. Synthesis of transactinide nuclei using radioactive beams (PDF). Physical Review C. 2007, 76 (1). 014612 [2021-12-02]. Bibcode:2007PhRvC..76a4612L. doi:10.1103/PhysRevC.76.014612. (原始内容 (PDF)存档于2018-12-03) (英语).
- ^ Modern alchemy: Turning a line (页面存档备份,存于互联网档案馆), The Economist, May 12, 2012.
- ^ 52.0 52.1 52.2 Superheavy Element Search Campaign at TASCA (页面存档备份,存于互联网档案馆). J. Khuyagbaatar
- ^ 53.0 53.1 53.2 Superheavy Element Search Campaign at TASCA (页面存档备份,存于互联网档案馆). Alexander Yakushev
- ^ 54.0 54.1 54.2 Khuyagbaatar, J.; Yakushev, A.; Düllmann, Ch. E.; et al. Search for elements 119 and 120 (PDF). Physical Review C. 2020, 102 (6). 064602 [25 January 2021]. Bibcode:2020PhRvC.102f4602K. S2CID 229401931. doi:10.1103/PhysRevC.102.064602. (原始内容 (PDF)存档于2021-12-09) (英语).
- ^ Search for element 119: Christoph E. Düllmann for the TASCA E119 collaboration (PDF). [2015-09-15]. (原始内容 (PDF)存档于2016-03-04) (英语).
- ^ 56.0 56.1 Ball, P. Extreme chemistry: experiments at the edge of the periodic table (PDF). Nature. 2019, 565 (7741): 552–555 [2021-12-02]. Bibcode:2019Natur.565..552B. ISSN 1476-4687. PMID 30700884. S2CID 59524524. doi:10.1038/d41586-019-00285-9
 . (原始内容 (PDF)存档于2019-04-12) (英语).
. (原始内容 (PDF)存档于2019-04-12) (英语). 延与秀人:“去年6月,我们已开始寻找第119号元素。这肯定需要很长时间,所以我们将每年间歇性地继续相同的实验100天或更长时间,直到我们或是其他人发现它。”
- ^ 57.0 57.1 57.2 Sakai, Hideyuki. Search for a New Element at RIKEN Nishina Center (PDF). infn.it. 2019-02-27 [2019-12-17]. (原始内容 (PDF)存档于2021-12-09) (英语).
- ^ Sakurai, Hiroyoshi. Greeting | RIKEN Nishina Center. 2020-04-01 [2021-12-02]. (原始内容存档于2021-12-02) (英语).
With the completion of the upgrade of the linear accelerator and BigRIPS at the beginning of 2020, the RNC aims to synthesize new elements from element 119 and beyond.
- ^ Hunt for element 119 set to begin. Chemistry World. 2017-09-12 [2018-01-09]. (原始内容存档于2020-11-11) (英语).
- ^ Chapman, Kit; Turner, Kristy. The hunt is on. Education in Chemistry. Royal Society of Chemistry. 2018-02-13 [2019-06-28]. (原始内容存档于2019-07-20) (英语).
The hunt for element 113 was almost abandoned because of lack of resources, but this time Japan’s emperor is bankrolling Riken’s efforts to extend the periodic table to its eighth row.
- ^ Scientists will begin experiments on the synthesis of element 119 in 2019. www.jinr.ru. JINR. 2016-09-28 [2017-03-31]. (原始内容存档于2021-12-02) (英语).
“The discovery of elements 115, 117 and 118 is an accomplished fact; they were placed in the periodic table, though still unnamed and will be confirmed only at the end of the year. The D.I.Mendeleev Periodic Table is not infinite. In 2019, scientists will begin the synthesis of elements 119 and 120 which are the first in the 8th period,” said S.N. Dmitriev.
- ^ Dmitriev, Sergey; Itkis, Mikhail; Oganessian, Yuri. Status and perspectives of the Dubna superheavy element factory (PDF). Nobel Symposium NS160 – Chemistry and Physics of Heavy and Superheavy Elements. 2016 [2021-12-02]. doi:10.1051/epjconf/201613108001
 . (原始内容 (PDF)存档于2021-08-28) (英语).
. (原始内容 (PDF)存档于2021-08-28) (英语).
- ^ What it takes to make a new element. Chemistry World. [2016-12-03]. (原始内容存档于2017-10-28) (英语).
- ^ Roberto, J. B. Actinide Targets for Super-Heavy Element Research (PDF). cyclotron.tamu.edu. Texas A & M University. 2015-03-31 [2017-04-28]. (原始内容 (PDF)存档于2016-03-10) (英语).
- ^ Morita, Kōsuke. The Discovery of Element 113. YouTube. 2016-02-05 [2017-04-28]. (原始内容存档于2021-12-02) (英语).
- ^ Morimoto, Kouji. The discovery of element 113 at RIKEN (PDF). 26th International Nuclear Physics Conference. 2016 [2017-05-14]. (原始内容 (PDF)存档于2021-12-09) (英语).
- ^ Hagino, Kouichi; Hofmann, Sigurd; Miyatake, Hiroari; Nakahara, Hiromichi. 平成23年度 研究業績レビュー(中間レビュー)の実施について [Implementation of the 2011 Research Achievement Review (Interim Review)] (PDF). www.riken.jp. RIKEN. July 2012 [2017-05-05]. (原始内容 (PDF)存档于2018-11-04) (日语及英语).
Of great advantage compared to other laboratories is the accessibility of long beam times for experiments at low cross-sections. Except at JINR in Dubna this situation is unique worldwide.
- ^ Chatt, J. Recommendations for the naming of elements of atomic numbers greater than 100. Pure and Applied Chemistry. 1979, 51 (2): 381–384. doi:10.1351/pac197951020381 (英语).
- ^ de Marcillac, Pierre; Coron, Noël; Dambier, Gérard; et al. Experimental detection of α-particles from the radioactive decay of natural bismuth. Nature. 2003, 422 (6934): 876–878. Bibcode:2003Natur.422..876D. PMID 12712201. S2CID 4415582. doi:10.1038/nature01541 (英语).
- ^ Considine, Glenn D.; Kulik, Peter H. Van Nostrand's scientific encyclopedia 9th. Wiley-Interscience. 2002. ISBN 978-0-471-33230-5. OCLC 223349096 (英语).
- ^ Chowdhury, P. Roy; Samanta, C.; Basu, D. N. Predictions of alpha decay half lives of heavy and superheavy elements. Nucl. Phys. A. 2007, 789 (1–4): 142–154. Bibcode:2007NuPhA.789..142S. CiteSeerX 10.1.1.264.8177
 . S2CID 7496348. arXiv:nucl-th/0703086
. S2CID 7496348. arXiv:nucl-th/0703086  . doi:10.1016/j.nuclphysa.2007.04.001 (英语).
. doi:10.1016/j.nuclphysa.2007.04.001 (英语).
- ^ Chowdhury, P. Roy; Samanta, C.; Basu, D. N. Search for long lived heaviest nuclei beyond the valley of stability. Phys. Rev. C. 2008, 77 (4). 044603. Bibcode:2008PhRvC..77d4603C. S2CID 119207807. arXiv:0802.3837
 . doi:10.1103/PhysRevC.77.044603 (英语).
. doi:10.1103/PhysRevC.77.044603 (英语).
- ^ Chowdhury, P. Roy; Samanta, C.; Basu, D. N. Nuclear half-lives for α -radioactivity of elements with 100 ≤ Z ≤ 130. Atomic Data and Nuclear Data Tables. 2008, 94 (6): 781–806. Bibcode:2008ADNDT..94..781C. arXiv:0802.4161
 . doi:10.1016/j.adt.2008.01.003 (英语).
. doi:10.1016/j.adt.2008.01.003 (英语).
- ^ Kratz, J. V. The Impact of Superheavy Elements on the Chemical and Physical Sciences (PDF). 4th International Conference on the Chemistry and Physics of the Transactinide Elements. 2011-09-05 [2013-08-27]. (原始内容 (PDF)存档于2017-01-06) (英语).
- ^ 75.0 75.1 75.2 75.3 75.4 Thayer, John S. Relativistic Effects and the Chemistry of the Heavier Main Group Elements. Maria, Barysz; Ishikawa, Yasuyuki (编). Relativistic Methods for Chemists. Challenges and Advances in Computational Chemistry and Physics 10. Springer Netherlands. 2010: 63–67, 81, 84. ISBN 978-1-4020-9974-8. doi:10.1007/978-1-4020-9975-5_2 (英语).
- ^ Fægri Jr., Knut; Saue, Trond. Diatomic molecules between very heavy elements of group 13 and group 17: A study of relativistic effects on bonding. The Journal of Chemical Physics. 2001, 115 (6): 2456. Bibcode:2001JChPh.115.2456F. doi:10.1063/1.1385366 (英语).
- ^ 77.0 77.1 77.2 Pyykkö, Pekka. A suggested periodic table up to Z ≤ 172, based on Dirac–Fock calculations on atoms and ions. Physical Chemistry Chemical Physics. 2011, 13 (1): 161–168 [2021-12-04]. Bibcode:2011PCCP...13..161P. PMID 20967377. S2CID 31590563. doi:10.1039/c0cp01575j. (原始内容存档于2021-10-19) (英语).
- ^ 78.0 78.1 Landau, Arie; Eliav, Ephraim; Ishikawa, Yasuyuki; Kador, Uzi. Benchmark calculations of electron affinities of the alkali atoms sodium to eka-francium (element 119). Journal of Chemical Physics. 2001-05-25, 115 (6): 2389–2392 [2015-09-15]. Bibcode:2001JChPh.115.2389L. doi:10.1063/1.1386413 (英语).
- ^ 79.0 79.1 Borschevsky, A.; Pershina, V.; Eliav, E.; Kaldor, U. Ab initio studies of atomic properties and experimental behavior of element 119 and its lighter homologs (PDF). The Journal of Chemical Physics. 2013-03-22, 138 (12). 124302 [2021-12-04]. Bibcode:2013JChPh.138l4302B. PMID 23556718. doi:10.1063/1.4795433. (原始内容 (PDF)存档于2022-03-15) (英语).
- ^ Lim, Ivan S.; Pernpointner, Markus; Seth, Michael; et al. Relativistic coupled-cluster static dipole polarizabilities of the alkali metals from Li to element 119. Physical Review A. 1999, 60 (4). 2822. Bibcode:1999PhRvA..60.2822L. doi:10.1103/PhysRevA.60.2822 (英语).
- ^ 81.0 81.1 81.2 Lavrukhina, Avgusta Konstantinovna; Pozdnyakov, Aleksandr Aleksandrovich. Analytical Chemistry of Technetium, Promethium, Astatine, and Francium. Translated by R. Kondor. Ann Arbor–Humphrey Science Publishers. 1970: 269. ISBN 978-0-250-39923-9 (英语).
- ^ 82.0 82.1 Jones, Cameron; Mountford, Philip; Stasch, Andreas; Blake, Matthew P. s-block Metal-Metal Bonds. Liddle, Stephen T. (编). Molecular Metal-Metal Bonds: Compounds, Synthesis, Properties. John Wiley and Sons. 2015-06-22: 23–24. ISBN 9783527335411 (德语).
- ^ 83.0 83.1 Seaborg. transuranium element (chemical element). Encyclopædia Britannica. c. 2006 [2010-03-16]. (原始内容存档于2010-11-30) (英语).
- ^ 84.0 84.1 Greenwood, N. N.; Earnshaw, A. Chemistry of the Elements 2nd. Oxford:Butterworth-Heinemann. 1997. ISBN 0-7506-3365-4.
- ^ Miranda, P. S.; Mendes, A. P. S.; Gomes, J. S.; et al. Ab Initio Correlated All Electron Dirac-Fock Calculations for Eka-Francium Fluoride (E119F). Journal of the Brazilian Chemical Society. 2012, 23 (6): 1104–1113 [2018-01-14]. doi:10.1590/S0103-50532012000600015
 (英语及葡萄牙语).
(英语及葡萄牙语).
- Audi, G.; Kondev, F. G.; Wang, M.; Huang, W. J.; Naimi, S. The NUBASE2016 evaluation of nuclear properties (PDF). Chinese Physics C. 2017, 41 (3): 030001. Bibcode:2017ChPhC..41c0001A. doi:10.1088/1674-1137/41/3/030001.
- Beiser, A. Concepts of modern physics 6th. McGraw-Hill. 2003. ISBN 978-0-07-244848-1. OCLC 48965418.
- Hoffman, D. C.; Ghiorso, A.; Seaborg, G. T. The Transuranium People: The Inside Story. World Scientific. 2000. ISBN 978-1-78-326244-1.
- Kragh, H. From Transuranic to Superheavy Elements: A Story of Dispute and Creation. Springer. 2018. ISBN 978-3-319-75813-8.
- Zagrebaev, V.; Karpov, A.; Greiner, W. Future of superheavy element research: Which nuclei could be synthesized within the next few years?. Journal of Physics: Conference Series. 2013, 420 (1). 012001. Bibcode:2013JPhCS.420a2001Z. ISSN 1742-6588. S2CID 55434734. arXiv:1207.5700
 . doi:10.1088/1742-6596/420/1/012001.
. doi:10.1088/1742-6596/420/1/012001.
- 元素Uue在Peter van der Krogt elements site的介绍(英文)
- WebElements.com – Uue(英文)

